
生命科学学院 新闻动态
癌症之所以难以攻克,很大程度上源于其内部复杂的生态系统。正如人类社会存在着不同族群一样,肿瘤组织内部也存在由基因突变等多种原因形成的亚克隆群体。这些亚克隆各具功能:有的擅长逃避免疫监视,有的疯狂掠夺营养,有的则善于扩散转移。这种被称为肿瘤内异质性(Intratumoral Heterogeneity,ITH)的现象,是癌症复发及当前治疗失败的关键原因之一。
肿瘤内部细胞群体的多样性构成了其复杂性的基础,而细胞间的特定信号通讯机制则推动了这些亚克隆之间的协同作用,从而促进肿瘤的整体进展。理解这种细胞间通讯网络,对于揭示肿瘤恶性转化的机制、开发新的治疗策略具有重要意义。
2025年8月22日,西湖大学生命科学学院/西湖实验室马仙珏课题组在《The EMBO Journal》发表了题为《Hemocytes facilitate interclonal cooperation-induced tumor malignancy by hijacking the innate immune system in Drosophila》的研究论文。该研究借助新型果蝇细胞间通讯肿瘤模型,揭示了异质性肿瘤与微环境中的免疫细胞通过细胞间通讯推动良性肿瘤向恶性表型转化的新机制。
文章链接:
https://doi.org/10.1038/s44318-025-00547-5
文章截图:

01 异质性RAS肿瘤遗传筛选新模型的建立
果蝇(Drosophila melanogaster)作为经典的模式生物,已被广泛应用于肿瘤发生与发展的机制研究。超过75%的人类疾病相关基因及关键信号通路在果蝇中均有对应的同源基因。与哺乳动物模型相比,果蝇具有生长周期短、饲养成本低等优势,且拥有丰富的遗传操作工具,便于开展大规模体内遗传筛选和高通量实验,是研究细胞间通讯与肿瘤微环境调控的理想模型。
癌基因RAS是人类癌症中突变率最高的驱动基因之一,在多种癌症中表现出高度异质性。然而,RAS突变克隆如何通过与肿瘤组织中的其它基因型细胞进行通讯,进而影响癌症发展,仍不清楚。
为了解决这一关键科学问题,马仙珏课题组在本研究中改进了经典的MARCM系统,构建了一个新型的RAS异质性肿瘤遗传筛选模型(图1)。利用该模型,结合EMS(甲基磺酸乙酯)这一化学诱变剂,研究人员能够在RAS肿瘤克隆的相邻细胞中特异性诱导随机基因X的纯合突变,从而观察X突变是否促进相邻RAS肿瘤的过度增殖。
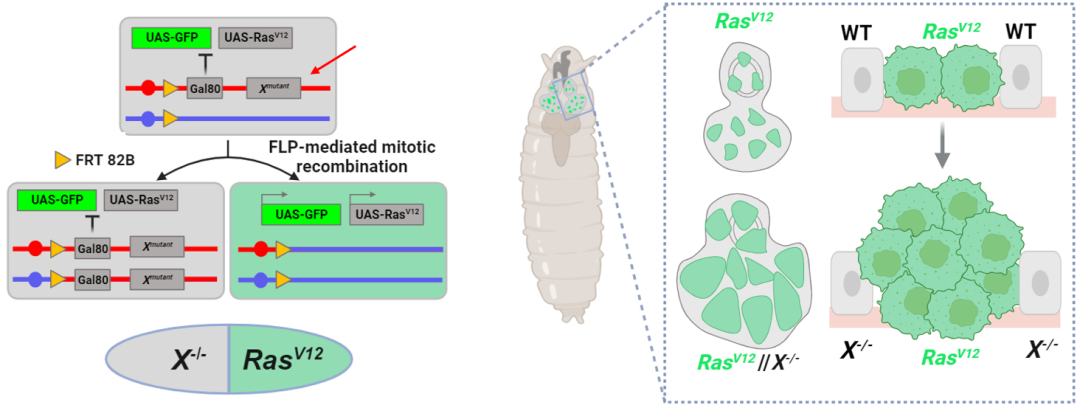
图1 克隆间合作诱导的异质性肿瘤模型的遗传学原理和示意图
通过系统的遗传筛选,研究人员发现三细胞连接蛋白M6的缺失会导致周围原本良性的RasV12肿瘤发展成为恶性肿瘤,并显著促进其增殖(图2)。尽管M6缺失本身会诱导细胞凋亡,但进一步研究表明,三细胞连接结构的破坏而非细胞凋亡,才是导致周围RasV12肿瘤恶性进展的关键原因。
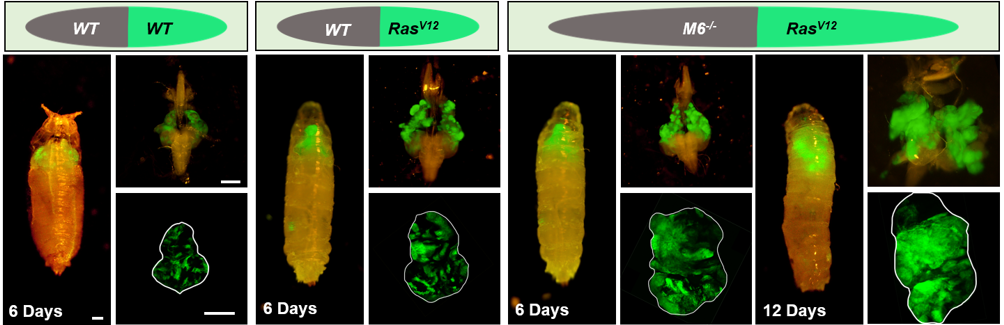
图2 M6-/-克隆促进相邻RasV12克隆转化为恶性肿瘤
02 肿瘤细胞间通讯新模型+单细胞测序:解析异质性肿瘤进展机制的新范式
为了深入解析异质性肿瘤进展的分子机制,研究团队将该肿瘤模型与单细胞转录组学技术相结合,构建了一种新的研究范式。一方面,该模型能够精准模拟体内肿瘤进展过程中的细胞间通讯,解决了传统转动物模型难以动态调控亚克隆协同作用的难题;另一方面,单细胞测序技术提供了对肿瘤微环境中不同细胞类型基因表达谱的高分辨率解析能力。
通过整合果蝇遗传学与单细胞转录组学的优势,研究团队揭示了RasV12//M6-/-异质性肿瘤与果蝇巨噬细胞(称为血细胞)之间动态互作的分子机制网络,主要包括以下几个关键发现:
1)肿瘤特异性分泌信号招募巨噬细胞。通过分析单细胞数据,研究团队发现RasV12//M6-/-肿瘤细胞特异性高表达血小板衍生生长因子同源蛋白Pvf1(果蝇中PDGF/VEGF家族成员)。通过构建转基因果蝇模型,研究人员敲除肿瘤中的Pvf1或阻断巨噬细胞中的Pvr受体,发现显著抑制巨噬细胞向肿瘤的浸润以及肿瘤的过度增殖。
2)巨噬细胞通过Spz-Toll通路促进肿瘤恶性转化。肿瘤组织免疫荧光染色的3D成像以及单细胞分析显示,被肿瘤募集的巨噬细胞高表达配体Spätzle(Spz),通过旁分泌的方式特异性地激活RasV12肿瘤细胞中的Toll先天性免疫信号通路,进而诱导恶性肿瘤的产生(图3)。
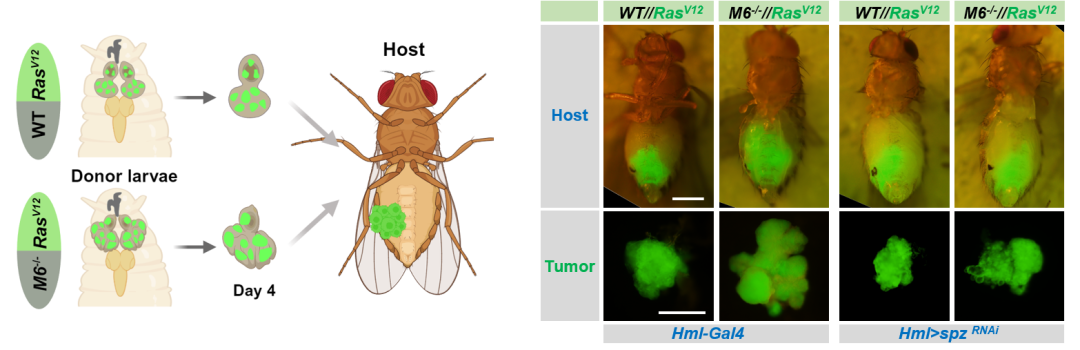
图3 巨噬细胞来源的Spz促进RasV12//M6−/−异质性肿瘤的过度增殖
3)JNK-Hippo信号级联的时空特异性调控。Toll通路激活后与RasV12协同,进一步激活下游的JNK-Hippo信号级联,促进肿瘤恶性转化。此外,研究团队发现肿瘤细胞中激活的JNK通路可上调Ets21C转录因子的表达,形成一个“Pvf1-Pvr/Spz-Toll/JNK-Ets21C”的正反馈环路,推动肿瘤进入失控增殖状态(图4)。
这一通讯机制揭示了肿瘤微环境中巨噬细胞的持续监测与动态响应能力,强调了细胞间通讯在异质性肿瘤恶性转化中的关键作用,为理解肿瘤-免疫互作提供了新的机制视角和潜在干预靶点。
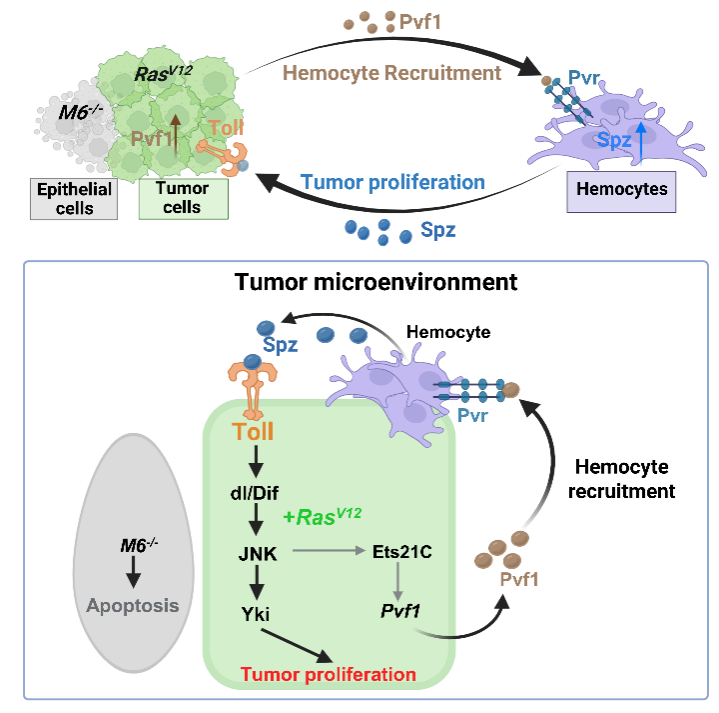
图4 果蝇巨噬细胞通过细胞间通讯促进RasV12//M6-/-异质性肿瘤的机制图
03 方法学创新与平台建设
本研究建立的果蝇异质性肿瘤模型具有重要的方法学价值。通过整合遗传操作、单细胞测序和功能基因组学,系统解析了异质性肿瘤介导的微环境重塑机制,为解析复杂肿瘤生态系统提供了可借鉴的研究范式。
此外,本研究通过改造果蝇MARCM系统,实现了多克隆肿瘤微环境的精准构建。结合优化的单细胞分离方案和生物信息学分析流程,研究团队成功解析了低丰度肿瘤相关巨噬细胞的转录特征并进行了体内功能验证。
最终,研究团队构建了一种基于QF/QUAS和GAL4/UAS系统的果蝇体内多器官基因编辑平台,实现了对肿瘤细胞与免疫细胞的系统化调控与同步检测,为深入解析肿瘤-免疫细胞交互作用及系统性病理进程提供了高效研究工具。
研究团队与资助情况
西湖大学生命科学学院/西湖实验室马仙珏研究员为本文通讯作者,课题组2020级博士生赵思华和郭一帆为文章的共同第一作者。研究工作得到了国家自然科学基金、西湖教育基金会及西湖实验室等项目的资助。
马仙珏课题组长期致力于肿瘤发生的分子机制研究,结合果蝇遗传学、细胞生物学和小鼠模型等多种手段,深入探究肿瘤发生发展过程中细胞间通讯及器官间通讯的分子机制。近年来,课题组在肿瘤微环境、器官间通讯、肿瘤信号转导等领域取得了一系列进展,相关研究发表于PNAS(2020, 2022),Developmental Cell,Cell Reports(2022a, 2022b,2023),Cell Research,EMBO Journal(2024,2025a, 2025b),Oncogene等国际知名学术期刊。
课题组热忱欢迎对肿瘤信号转导、细胞间通讯、器官间通讯或果蝇遗传学等研究方向感兴趣的有志之士(博士后、科研助理、博士生)加入,共同探索生命科学前沿,享受科研创新的乐趣!
















