
生命科学学院 新闻动态
溶瘤病毒疗法(Oncolytic virus, OV)是一种新型肿瘤治疗方法。该疗法通过基因工程技术改造天然病毒,使其具备特异性感染肿瘤细胞的能力。改造后的病毒不仅能直接裂解肿瘤细胞,还可释放肿瘤抗原和病毒抗原,从而激活抗病毒免疫应答和抗肿瘤免疫应答。尽管临床试验已证实溶瘤病毒疗法对胶质母细胞瘤(Glioblastoma, GBM)具有一定的治疗潜力,但部分患者对此疗法响应较弱或完全无响应,提示GBM中可能存在关键基因的调控作用,导致肿瘤细胞对治疗产生耐药性。因此,系统解析GBM中溶瘤病毒疗法耐药相关基因及其作用机制,将为提升该疗法的临床疗效提供重要理论依据。
北京时间2025年7月30日,西湖大学生命科学学院谢琦团队、中国医学科学院系统医学研究院/苏州系统医学研究所王宸团队、上海交通大学系统生物医学研究院蔡宇伽团队合作在Cell Reports Medicine杂志发表了题为“BRD9 inhibition overcomes oncolytic virus therapy resistance in glioblastoma”的研究论文。该研究通过CRISPR/Cas9高通量基因筛选技术,首次揭示BRD9通过调控抗病毒基因表达,影响溶瘤病毒在胶质母细胞瘤中的治疗效果。
文章链接:
https://www.cell.com/cell-reports-medicine/fulltext/S2666-3791(25)00331-3
文章截图:

该研究通过全基因组CRISPR/Cas9筛选技术,发现BRD9是调控溶瘤病毒oHSV1对胶质母细胞瘤治疗效果的关键基因。进一步实验表明,敲除BRD9显著促进oHSV1在胶质瘤细胞内的复制效率,并增强其杀伤作用(图1)。
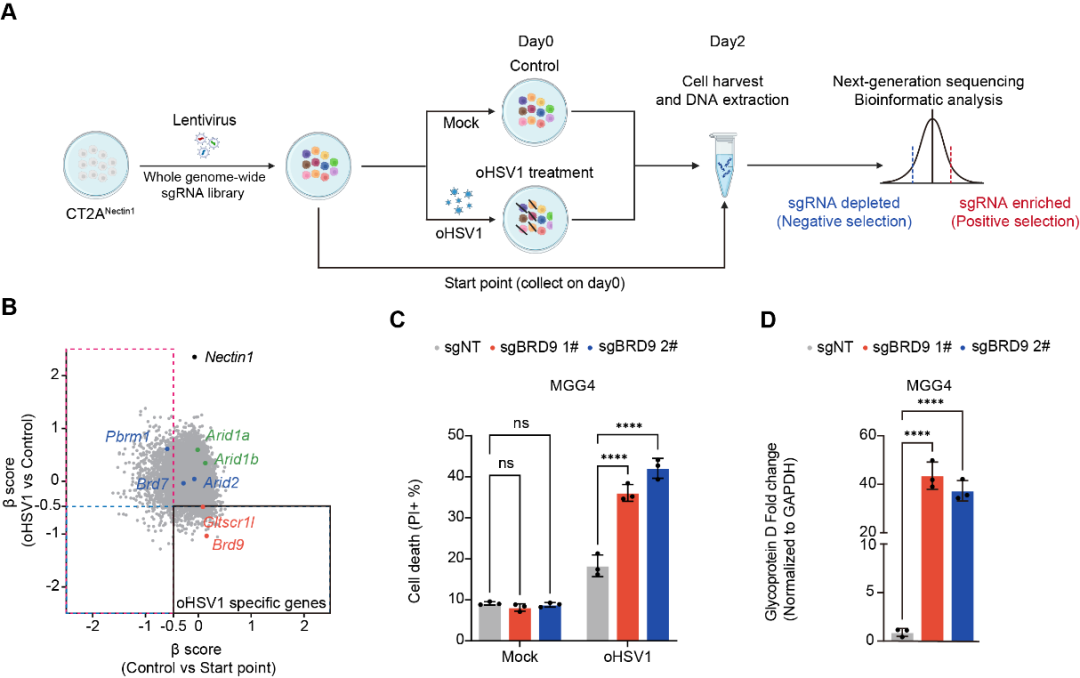
图1:CRISPR/Cas9筛选发现BRD9是影响溶瘤病毒治疗效果的关键基因
为阐明BRD9调控胶质瘤细胞对oHSV1产生抵抗的分子机制,研究团队结合RNA-seq、ChIP-seq及内源性免疫共沉淀(CO-IP)技术,发现BRD9通过调控NF-κB信号通路关键转录因子RELA,促进相关下游抗病毒基因的表达,从而显著抑制oHSV1在肿瘤细胞内的复制能力,并降低其对肿瘤细胞的杀伤作用(图2)。
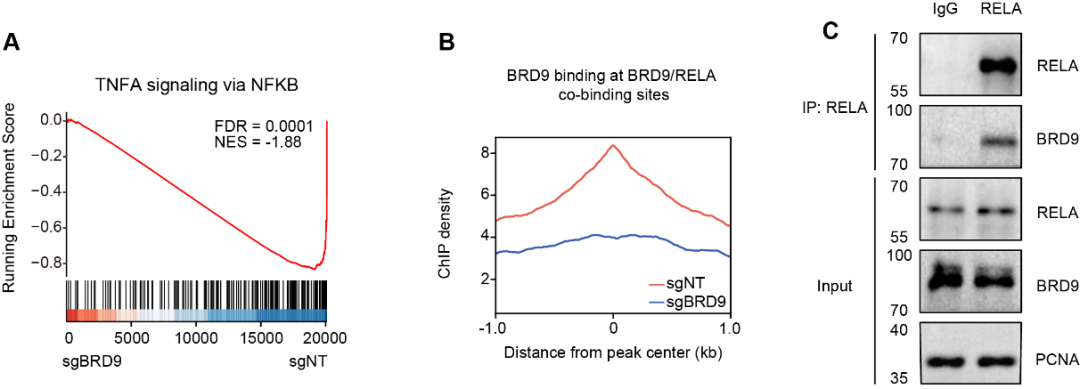
图2:BRD9通过调控RELA影响抗病毒基因表达
研究团队通过胶质瘤肿瘤类器官、胶质瘤肿瘤切片培养物及小鼠原位胶质瘤模型等多种体外和体内模型,系统性评估了BRD9的作用效果。研究发现,采用BRD9小分子抑制剂IBRD9联合oHSV1治疗,可显著增强HSV1在多种模型中的复制及杀伤作用,疗效优于单独使用oHSV1。同时在小鼠原位胶质瘤模型中,联合应用IBRD9、oHSV1及免疫检查点抑制剂(PD-1和CTLA-4抑制剂)进一步显著延长了小鼠生存期,并展现出卓越的抗肿瘤功效(图3)。
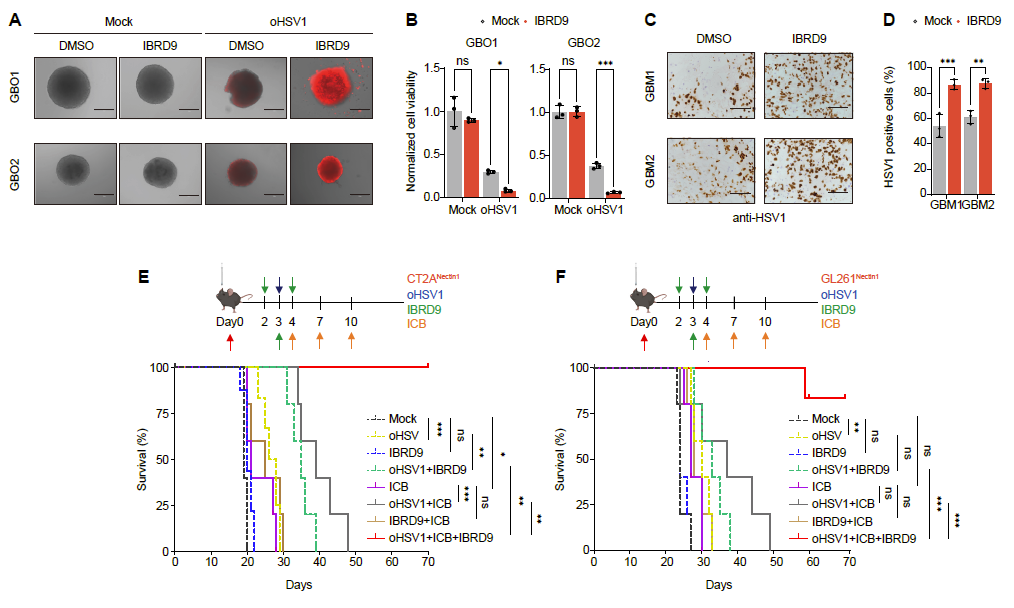
图3:靶向抑制BRD9可显著增强oHSV1的治疗效果
综上所述,该研究通过CRISPR/Cas9全基因组筛选方法,发现BRD9通过调控NF-κB信号通路介导的抗病毒反应,显著影响溶瘤病毒oHSV1对胶质母细胞瘤的治疗效果。敲除或靶向抑制BRD9可显著增强oHSV1在胶质瘤细胞内的复制能力及杀伤作用。这项研究为提升溶瘤病毒在胶质母细胞瘤中的治疗效果提供了重要理论依据(图4)。
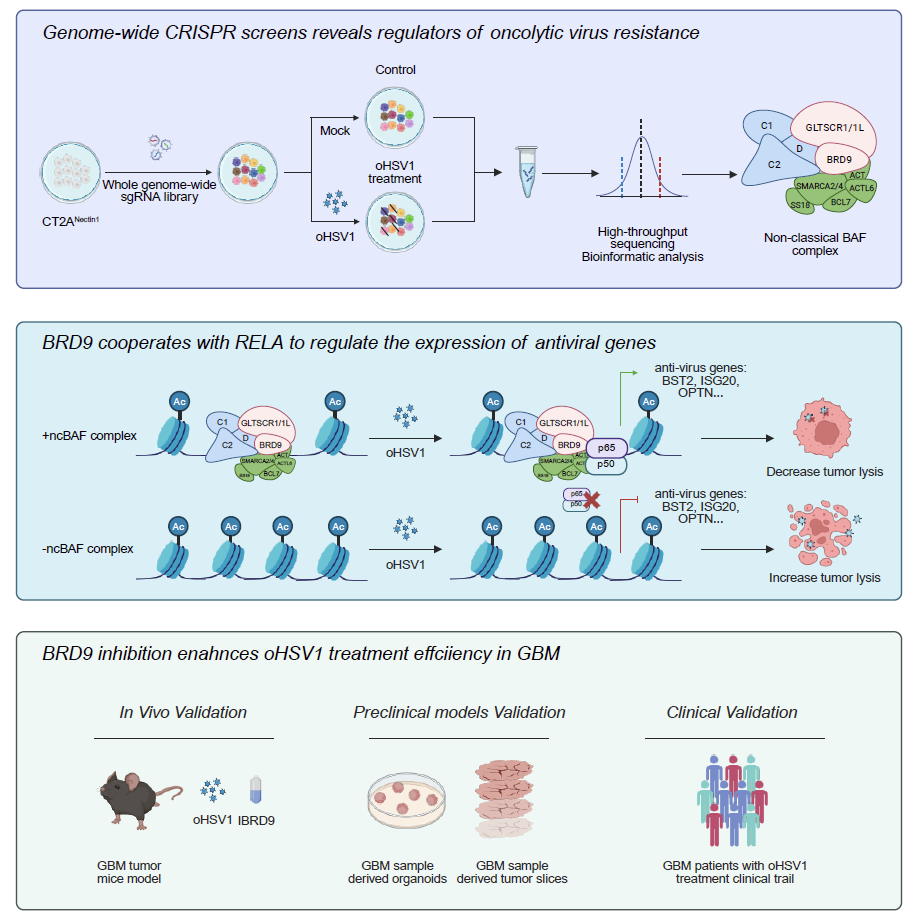
图4:研究内容模式图
西湖大学生命科学学院谢琦研究员、中国医学科学院系统医学研究院/苏州系统医学研究所王宸研究员、上海交通大学蔡宇伽研究员为本文共同通讯作者,西湖大学博士研究生郭琛、龙志林、林鹏为本文共同第一作者。本研究得到了国家自然科学基金和西湖教育基金会、以及浙江省“尖兵”和“领雁”研发计划的资金支持。本研究还得到浙江大学第一医院肝胆胰外科沈艺南主任的大力帮助。
西湖大学生命科学学院谢琦课题组一直从事脑肿瘤的靶向和免疫治疗研究,取得了一系列的研究成果,近5年以通讯作者(含共同)在Cell, Nature Biomedical Engineering, Cancer Discovery, Immunity等杂志发表研究论文,合作发起一项IIT临床实验。
详情见实验室主页:https://xieqi.lab.westlake.edu.cn/。欢迎优秀人才加入我们的研究团队推动相关课题。有意者可以联系谢琦博士(xieqi@westlake.edu.cn)。
最新资讯
人物故事
大学新闻
大学新闻
















